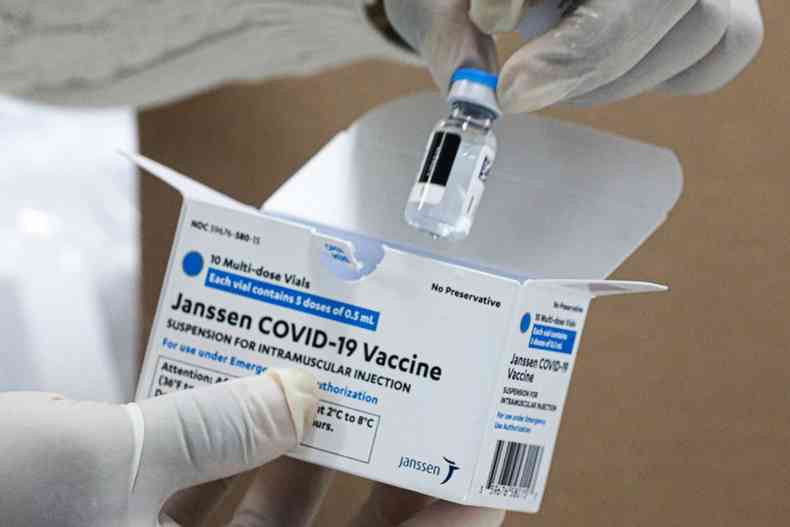
Um vídeo publicado no Instagram engana ao relacionar a extensão da validade de vacinas da Janssen, subsidiária da Johnson & Johnson, com a doação de doses pelos Estados Unidos para outros países – incluindo o Brasil.
Como verificamos?
Verificação
Suspensão temporária das vacinas Johnson & Johnson
As of 4/12, 6.8m+ doses of the J&J vaccine have been administered in the U.S. CDC & FDA are reviewing data involving 6 reported U.S. cases of a rare & severe type of blood clot in individuals after receiving the vaccine. Right now, these adverse events appear to be extremely rare
%u2014 U.S. FDA (@US_FDA) April 13, 2021
Conclusão
Following a thorough safety review, the FDA and @CDCgov have determined that the recommended pause regarding the use of the Johnson & Johnson (Janssen) #COVID19 Vaccine in the U.S. should be lifted and use of the vaccine should resume. https://t.co/QSuse0jyas pic.twitter.com/cdIH1yHa8s
%u2014 U.S. FDA (@US_FDA) April 23, 2021